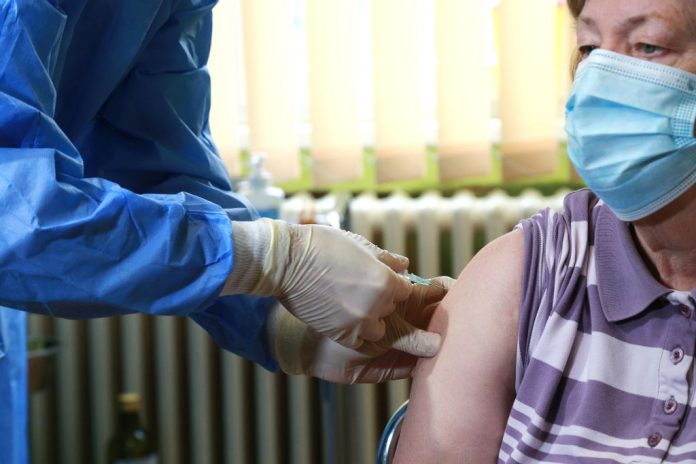
U otvorenom pismu objavljenom 12. ožujka skupina od 12 istaknutih znanstvenika i liječnika zatražila je da Europska agencija za lijekove (EMA) odgovori na “hitna” sigurnosna pitanja o tri COVID-19 cjepiva koja su odobrena za uporabu u EU ili da povuku odobrenja za njihovo korištenje, donosi LifeSiteNews.
U otvorenom pismu skupina znanstvenika postavila je pitanje “Je li EMA na odgovarajući način adresirala glavna pitanja u vezi sigurnosti cjepiva prije njihovog odobrenja?”
Naime, EMA je odobrila tri cjepiva za hitnu upotrebu u EU: Pfizer-BioNtech, Moderna i Oxford-AstraZeneca.
U svom pismu 12 znanstvenika i liječnika istaknulo je da je nakon cijepljenja cjepivima protiv COVID-19 na genskoj osnovi prijavljen “širok raspon nuspojava” kod prethodno zdravih mlađih osoba.
Napisali su:
Postoje brojni medijski izvještaji iz cijelog svijeta o staračkim domovima koje je COVID-19 poharao nekoliko dana nakon cijepljenja njihovih korisnika. Iako je moguće da se svaki od ovih događaja mogao dogoditi uslijed nesretne slučajnosti, zabrinuti smo što se do sada nisu provodila i još uvijek se ne provode odgovarajuća ispitivanja mogućih uzroka bolesti ili smrti u tim okolnostima, posebice zbog izostanka obdukcija.
U svom originalnom pismu, poslanom EMA-i 28. veljače e-mailom, skupina je zatražila od EMA-e: „U roku od sedam dana odgovorite na sedam pitanja vezanih uz sigurnost, a koja izazivaju zabrinutost. Ukoliko se ne odlučite udovoljiti ovom razumnom zahtjevu, objavit ćemo ovo pismo javnosti.”
Prema izvještaju organizacije Children’s Health Defense neki navodi iz pisma u vezi nuspojava su trombocitopenija, ozljede endotela, mikrotrombi i moždani udar.
Autori, predvođeni s dr. Sucharit Bhakdi, profesorom emeritusom medicinske mikrobiologije i imunologije i bivšim predsjednikom Instituta za medicinsku mikrobiologiju i higijenu Johannes Gutenberg Sveučilišta u Meinzu, još nisu dobili odgovor od EMA-e.
U pismu su izjavili:
„Kao polaznu točku smatramo važnim nabrojati i provjeriti sve smrtne slučajeve koji su se dogodili u roku od 28 dana nakon cijepljenja te usporediti kliničke slike s onima koji nisu cijepljeni.
Opširnije, s obzirom na razvoj cjepiva COVID-19, Parlamentarna skupština Vijeća Europe izjavila je u svojoj Rezoluciji 2361 od 27. siječnja 2021. da države članice moraju osigurati da sva cjepiva COVID-19 budu podržana visokokvalitetnim ispitivanjima koja su provedena na ispravan i etičan način. Predstavnici EMA-e i druga regulatorna tijela u zemljama EU-a obvezana su primijeniti ove kriterije. Trebaju biti svjesni da možda krše Rezoluciju 2361 ukoliko primjenjuju medicinske proizvode koji su još uvijek u trećoj fazi ispitivanja.
Prema Rezoluciji 2361 države članice također moraju obavijestiti građane da cijepljenje NIJE obvezno i osigurati da nitko ne vrši politički, socijalni ili drugi pritisak na cijepljenje. Države se moraju pobrinuti i da nitko ne bude diskriminiran zbog ne-cijepljenja.“
Dr. Bhakdi je također objavio video izjavu u kojoj kaže: “Vrijeme da vlade djeluju, vrijeme da svi djeluju je sada”.
U nastavku je sedam “hitnih” sigurnosnih pitanja ove skupine znanstvenika i liječnika na koja traže odgovor EMA-e:
- Očekivano je da će cjepiva napravljena na genetskoj osnovi nakon intramuskularne injekcije dospjeti u krvotok i raširiti se po tijelu. Zahtijevamo dokaze da je ta mogućnost isključena u pretkliničkim ispitivanjima na životinjama na sva tri cjepiva prije nego što ih je EMA odobrila za upotrebu na ljudima.
- Ako takvi dokazi nisu dostupni, očekivano je da će cjepiva ostati zarobljena u cirkulaciji i da će ih apsorbirati endotelne stanice. Može se pretpostaviti da će se to dogoditi osobito na mjestima usporenog protoka krvi, tj. u malim žilama i kapilarama. Zahtijevamo dokaze da je ta vjerojatnost isključena u pretkliničkim ispitivanjima na životinjama na sva tri cjepiva prije odobrenja EMA-e za upotrebu na ljudima.
- Ako takvi dokazi nisu dostupni, očekivano je da će tijekom ekspresije nukleinskih kiselina iz cjepiva, peptidi šiljastih proteina biti prezentirani putem MHC I kompleksa na luminalnoj površini stanica. Mnoge zdrave osobe imaju CD8-limfocite koji prepoznaju takve peptide, što je možda posljedica prethodne infekcije COVID-om, ali i unakrsnih reakcija s drugim vrstama koronavirusa. Moramo pretpostaviti da će ovi limfociti napadati te stanice. Zahtijevamo dokaze da je ta vjerojatnost isključena u pretkliničkim ispitivanjima na životinjama na sva tri cjepiva prije nego što ih je EMA odobrila za upotrebu na ljudima.
- Ako takvi dokazi nisu dostupni, očekivano je da će na bezbrojnim mjestima u tijelu nastupiti oštećenje endotela te koagulacija krvi radi aktivacije trombocita. Zahtijevamo dokaze da je ta vjerojatnost isključena u pretkliničkim ispitivanjima na životinjama na sva tri cjepiva prije nego što ih je EMA odobrila za upotrebu na ljudima.
- Ako takvi dokazi nisu dostupni, očekivano je će to dovesti do pada broja trombocita i pojave D-dimera u krvi te do bezbrojnih ishemijskih lezija u cijelom tijelu uključujući mozak, leđnu moždinu i srce. Pojavom ove nove vrste DIK-sindroma (diseminirana intravaskularna koagulacija) mogu se javiti poremećaji krvarenja uključujući između ostaloga i obilna krvarenja te hemoragični moždani udar. Zahtijevamo dokaze da su sve te mogućnosti isključene u pretkliničkim ispitivanjima na životinjama na sva tri cjepiva prije nego što ih je EMA odobrila za upotrebu na ljudima.
- SARS-CoV-2 šiljasti protein veže se na ACE2 receptor na trombocitima što rezultira njihovom aktivacijom. U težim slučajevima infekcije SARS-CoV-2 zabilježena je trombocitopenija (smanjeni broj trombocita u krvi). Trombocitopenija je također zabilježena u cijepljenih osoba. Zahtijevamo dokaze da je ova potencijalna opasnost od aktivacije trombocita koja može dovesti do DIK-sindroma isključena na sva tri cjepiva prije nego što ih je EMA odobrila za upotrebu kod ljudi.
- Širenje SARS-CoV-2 diljem svijeta stvorilo je pandemiju bolesti povezanu s mnogim smrtnim ishodima. Međutim, do trenutka razmatranja zahtjeva za odobrenje cjepiva zdravstveni sustavi većine zemalja više nisu bili pod neposrednom prijetnjom od preopterećenja jer je velik dio svijeta već bio zaražen, a najgora pandemija je bila popustila. Slijedom toga, zahtijevamo uvjerljive dokaze da je hitnost postojala u vrijeme kada je EMA izdala uvjetno odobrenje za stavljanje lijeka/cjepiva u promet proizvođačima sva tri cjepiva, kako bi opravdala odobrenje cjepiva za upotrebu na ljudima od strane EMA-e, zbog takve navodne hitnosti. Inače, uvjetno odobrenje za stavljanje lijeka u promet je ubrzani postupak u kojem se prilaže dokumentacija koja ne sadrži uobičajen opseg podataka o lijeku, ukoliko korist od ranije dostupnosti lijeka bolesnicima nadmašuje rizike trenutačnog nedostatka potpunih podataka o tome lijeku.
*Članak je preveo Domagoj Beg
Tekst se nastavlja ispod oglasa

































































